- 首页 > 正文
周晓霜教授:木村病及相关肾损害的诊治进展【下篇】
发表时间:2024-12-09 16:43:31
编者按:木村病(Kimura disease,KD)又称嗜酸性粒细胞增多性肉芽肿,是一种罕见的良性慢性炎症性疾病,病因不明,大部分的病例报道发生在亚裔人群。木村病最常见的表现是头颈部无痛性淋巴结肿大或皮下肿块,有12%~16%的患者可有肾脏受累,特别容易表现为肾病综合征。因此,对于木村病的诊治,肾脏科医生也应掌握。本刊特邀山西省人民医院周晓霜教授基于一例木村病相关肾损害病例的诊疗过程,详细阐述了木村病的诊治进展以及木村病相关肾损害的诊断及治疗。我们将分上、下两篇与您分享,希望能为广大肾脏科医生的临床实践带来裨益。本文为下篇。
一、木村病的诊治进展
(一)定义及病因
木村病(Kimura disease,KD;木村病)又称为嗜酸粒细胞增生性淋巴肉芽肿。
中国学者金显宅1937年在中华医学会杂志首次报道7例嗜酸性粒细胞增生性肉芽肿病例;1948年日本学者Kimura等人发表了题为《论合并淋巴组织增生改变的不寻常肉芽肿》,对该病进行了详细的描述,后续文献多将该病称为木村病。目前有文献记载的病例以亚洲男性多见,男女发病比例(3.5~9):1,发病年龄为4~80岁,多发生于20~40岁。该病是一种以无痛性皮下结节或肿物为主要表现的慢性炎症性疾病,主要累及耳周及颌下区,也可以出现在其他淋巴结区受累表现,病理上主要表现为淋巴结中嗜酸性淋巴肉芽肿,部分伴不同程度脓肿甚至坏死。
木村病的病因及发病机制尚不明确,推测可能与过敏反应、自身免疫反应、感染有关。
(二)临床表现
临床上木村病多表现为皮下软组织进行性无痛性肿大包块,好发于头颈部,易累及涎腺和/或区域淋巴结。多为单侧发病。
主要症状:常见于眼睑、泪腺、眶周、颊部、腹股沟、前臂、腋窝、纵隔,也偶有发生在臀部等部位。表现为进行性、无痛性增大的包块,直径1~20 cm不等,界限不清,严重时可致面部畸形。病变处皮肤可有瘙痒和色素沉着。
淋巴结病症:约有30%~40%的患者伴发淋巴结病变。
肾脏病症:木村病患者中约12%~16%的病变累及肾脏,可表现为肾病综合征。肾脏病变可在皮下肿物出现后发生(较多见),也可同时发生。
其他症状:部分患者还伴有湿疹、哮喘、溃疡性结肠炎、血管炎、嗜酸性心肌炎、嗜酸性脂膜炎、分泌性中耳炎,同时可观察到有雷诺现象。
(三)诊断
根据临床表现及外周血嗜酸性粒细胞和IgE水平升高,亚裔患者应考虑木村病的可能。伴发肾脏疾病的患者中,可能有IgG4升高、血沉加快、白细胞增多、C反应蛋白升高等现象。
影像学检查可了解病变部位、血管情况、与周围组织关系。
①超声表现为软组织内边界不清楚的肿块,形态不规则,回声不均匀,可见条状高回声分布于低回声内,称为“木纹样”改变,部分与皮肤分界不清。
②CDFI:血流丰富,常伴有周围多发淋巴结肿大,肿大淋巴结主要表现为皮质增厚,淋巴门缩小或显示不清,内回声不均,可见多发微小的更低回声区域,血流既可以呈门型丰富血流,也可以紊乱。
③术前的CT和MRI有助于行病灶切除时的定位及明确肿物对周围软组织的累及范围。
病理学诊断
木村病需依靠活组织病理检查确诊(图3)。其特点如下:
①病变多呈灰黄或灰白色,病变无被膜,与周围组织无明显边界。
② 病变侵犯真皮层和肌肉;
③炎症细胞增生和浸润,病变组织可见广泛的淋巴滤泡样结构,大量的嗜酸性粒细胞、 淋巴细胞及肥大细胞充斥于滤泡间,多形成嗜酸性微脓肿(特征性改变);
④血管增生反应;
⑤不同程度的纤维化;
⑥免疫组化:淋巴滤泡以B细胞为主,而滤泡间以T细胞为主,生发中心内的嗜伊红色沉积物主要为IgE。
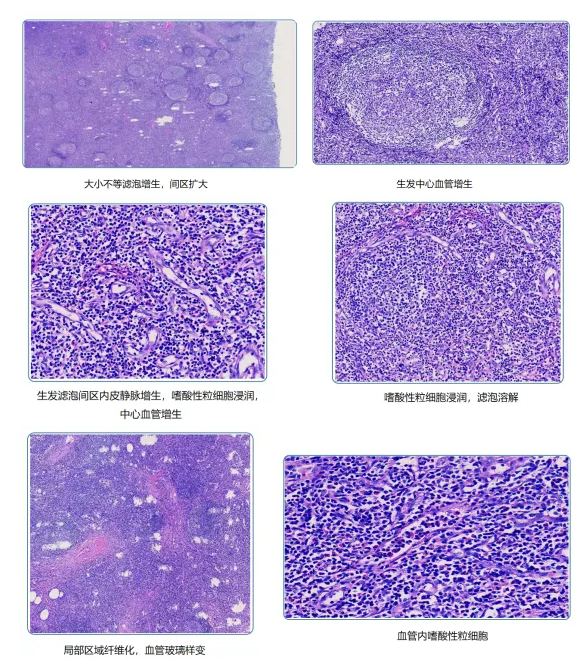
图3. 木村病的典型病理表现
对于多部位受累的木村病患者,存在活检病理部位的选择问题。头颈部作为常见受累部位,是活检首选部位,但却因为可能影响容貌,容易受到患者抵触。腹股沟淋巴结也是木村病的常见受累部位,且活检相对安全,但腹股沟淋巴结肿大特异性差,故在临床中常不被推荐。
2019年北京协和医院对46例患者的回顾性研究中,共17例因淋巴结活检确诊,其中7例(41.2%)通过腹股沟淋巴结活检确诊木村病,这一结果提示木村病患者中腹股沟淋巴结受累阳性率并不低,且因为其安全性可作为活检的首选。
(四)鉴别诊断
对于淋巴结肿大患者应注意区分病因,包括:感染、肿瘤、反应性增生、细胞代谢异常等。
有代表性的几种疾病如下:
血管淋巴样增生伴嗜酸性粒细胞增多症(ALHE):好发于头颈部,多表现为丘疹或红色结节,是一种良性血管增生性病变。ALHE与木村病非常相似,但ALHE病理以血管增生病变为主,增生的血管内皮细胞呈特征性的上皮样,而淋巴滤泡少见。
淋巴结结核:有淋巴结肿大、低热、盗汗等结核感染中毒症状,血沉增快,PPD试验强阳性,T-spot阳性,淋巴结病理可见干酪样坏死灶,抗酸染色阳性。
淋巴瘤:可表现为淋巴结肿大,伴有发热、乏力、体重明显下降,乳酸脱氢酶明显升高等,淋巴结病理可见淋巴结结构破坏,单克隆性B或T淋巴细胞增生,霍奇金淋巴瘤可见镜影细胞。
Castelman病:是一种淋巴增殖性疾病,表现为单发或全身多发的淋巴结肿大,其中颈部肿大淋巴结发生率较高,无嗜酸性粒细胞增多、IgE升高表现,淋巴结病理可见特征性“洋葱皮”样外观及“棒棒糖”结构。
血管免疫母细胞性淋巴结病:可表现为淋巴结肿大,但多为全身,且伴有发热、肝脾肿大、皮肤损害、高丙种球蛋白血症等表现。淋巴结病理可见淋巴结结构破坏,树枝状小血管增生伴内皮细胞增生肿胀。
(五)治疗
1.手术治疗
手术治疗是症状性患者的一线治疗,主要用于肿瘤减积或取材活检。由于其浸润性生长、界限不清,手术切除难以达到切缘阴性,导致手术切除术后复发率高,约为25%。
2.药物治疗
包括全身或局部的激素治疗、非甾体抗炎药、细胞毒性药物、环孢素、硫唑嘌呤、伊马替尼、免疫球蛋白等,疗效不一。
奥马珠单抗是一种抗IgE单克隆抗体,Nonaka等报告使用奥马珠单抗治疗3例手术治疗无法控制的KD患者获得成功,肿块体积缩小,外周血嗜酸性粒细胞和嗜碱性粒细胞计数减少。
3.生物制剂
Huang HY等在2022年首次报告一例伴有腹部和小腿慢性湿疹的36岁男性患者因左股部进行性增大的肿块接受手术切除,术后诊断为KD,患者接受了度普利尤单抗治疗8个月(初始600 mg,此后每2周300 mg),治疗4个月时皮损显著缩小,随访1年未复发。
Bellinato F等报告一例59岁塞内加尔男性KD患者病程长达20年,曾多次接受糖皮质激素、四环素类、吲哚美辛和氨苯砜治疗无效,实验室检查示外周血嗜酸性粒细胞百分数(15%)和血清IgE水平(800 UI/mL)升高。患者接受了度普利尤单抗300 mg皮下注射,每2周一次,治疗2个月后瘙痒完全缓解,皮下结节逐渐变平,遗留色素沉着,6个月随访未复发。
4.放射治疗
对于停用糖皮质激素后再次复发的病例,或肿物已对糖皮质激素产生耐药性的病例,可以考虑使用放射治疗。
对病变范围广、多发且边界不清的患者,首选放疗,而且对术后或放疗后复发的患者,再次放疗仍有效。
放射治疗的副作用较多,应尽量避免应用于年轻患者。
5.其他治疗
例如激光、冷冻试验性治疗。
(六)预后
该病属于良性病变,预后较好,但有较高复发率。
复发可能受多种因素的影响,如病程、病变大小、单发或多发、病变边界的清晰程度、外周血嗜酸性粒细胞及IgE水平。
有研究报道,病变范围>3.5 cm,外周血嗜酸性粒细胞百分比>50%,血IgE>10 000 IU/ml,Notch-1表达阳性或Ki-67增多的病人更容易复发,Notch-1和Ki-67可能是该病复发的预测指标。
二、木村病相关肾损害
木村病合并肾脏受累并不少见,12%~16%的患者有蛋白尿,其中59%~100%可表现为肾病综合征。肾损害常出现在木村病的肾外表现之后或同时发生。
目前所报道的木村病相关的肾损害病理类型多种多样,包括膜性肾病、微小病变性肾病、系膜增生性肾小球肾炎、局灶节段硬化性肾小球病、IgM或IgA肾病等,缺乏特异性。有个案报道肾活检可见部分伴有间质小管中单个核细胞和嗜酸性粒细胞浸润。
(一)木村病相关肾损害的病因及发病机制
有研究发现,伴有肾脏受累的木村病患者外周血CD4+和CD8+T细胞计数明显升高,提示辅助T细胞(Th细胞)参与疾病的发生发展过程。Th2分泌的白细胞介素4可诱导嗜酸性粒细胞聚集,并促进B细胞产生IgE。血嗜酸性粒细胞升高及高水平IgE引起的高敏状态可进一步干扰Th2细胞功能,并释放多种细胞因子,导致足细胞内相关信号通路活化,破坏足细胞骨架蛋白结构和细胞间连接蛋白,增加肾小球基底膜的通透性,引起蛋白尿。
(二)木村病相关肾损害的鉴别诊断
肾病综合征合并淋巴结肿大其他病因需鉴别如下:
1.淋巴增殖性疾病:包括淋巴瘤、Castleman病、POEMS综合征等。
淋巴瘤:常有发热、盗汗、体重减轻等表现,肝脾可肿大,组织病理可协助鉴别; Castleman病可有发热、乏力、红细胞沉降率增快等表现,常伴IL-6、VEGF水平升高,组织病理可协助鉴别;
POEMS综合征:该病诊断以多发神经病变、单克隆免疫球蛋白血症为必要条件,伴有皮肤及内分泌病变。
2.自身免疫疾病
自身免疫疾病可有乏力、口干、眼干、皮疹、关节疼痛等表现,且多表现为多系统受累,血中可检测到特异性自身免疫抗体。
3.实体肿瘤
实体肿瘤多见于老年人,可有体重减轻、贫血等消耗症状,可有肿瘤标记物的升高,影像学检查可发现实体肿瘤灶。
4.IgG4相关疾病
常表现为自身免疫性胰腺炎、硬化性胆管炎和/或唾液腺、泪腺肿大,伴血IgG4升高,组织病理学检查发现密集淋巴浆细胞浸润、席纹状纤维化和闭塞性静脉炎是主要诊断特征。
5.感染性疾病
常有发热及其他系统感染的表现,如咳嗽、咳痰、腹痛、腹泻、皮肤红肿等,常伴有炎症指标升高,病原学检查阳性。
(三)木村病相关肾损害的治疗
木村病合并肾病综合征患者首选全身应用激素治疗,对于复发或激素耐药患者需应用激素联合免疫抑制剂治疗。
为预防木村病复发或有肾脏等其他脏器受累,部分病例报道在糖皮质激素减量时,可加用免疫抑制剂,常用免疫抑制剂包括环磷酰胺、吗替麦考酚酯、环孢素、他克莫司等。
也有在个别肾脏受累患者中发现,即使联合糖皮质激素及免疫抑制剂仍可能无法有效控制病情,但当手术切除皮下受累肿块后,患者的膜性肾病也可很快得到缓解。
专家简介

周晓霜 教授
山西省人民医院肾内科
主任医师,博士研究生导师,省优专家
肾脏重症病区主任
山西省肾脏病大数据中心常务副主任
医学博士,美国贝勒医学院肾内科博士后
太原理工大学大数据学院博士后
主持国家自然科学基金3项,主持山西省优秀青年基金
获 “中共山西省委组织部山西省青年拔尖人才”、 “山西省人民政府嘉奖” 、“山西省学术技术带头人”“三晋英才拔尖骨干人才”、“山西省五四青年奖章”、“山西省青年岗位能手”等荣誉。
一、木村病的诊治进展
(一)定义及病因
木村病(Kimura disease,KD;木村病)又称为嗜酸粒细胞增生性淋巴肉芽肿。
中国学者金显宅1937年在中华医学会杂志首次报道7例嗜酸性粒细胞增生性肉芽肿病例;1948年日本学者Kimura等人发表了题为《论合并淋巴组织增生改变的不寻常肉芽肿》,对该病进行了详细的描述,后续文献多将该病称为木村病。目前有文献记载的病例以亚洲男性多见,男女发病比例(3.5~9):1,发病年龄为4~80岁,多发生于20~40岁。该病是一种以无痛性皮下结节或肿物为主要表现的慢性炎症性疾病,主要累及耳周及颌下区,也可以出现在其他淋巴结区受累表现,病理上主要表现为淋巴结中嗜酸性淋巴肉芽肿,部分伴不同程度脓肿甚至坏死。
木村病的病因及发病机制尚不明确,推测可能与过敏反应、自身免疫反应、感染有关。
(二)临床表现
临床上木村病多表现为皮下软组织进行性无痛性肿大包块,好发于头颈部,易累及涎腺和/或区域淋巴结。多为单侧发病。
主要症状:常见于眼睑、泪腺、眶周、颊部、腹股沟、前臂、腋窝、纵隔,也偶有发生在臀部等部位。表现为进行性、无痛性增大的包块,直径1~20 cm不等,界限不清,严重时可致面部畸形。病变处皮肤可有瘙痒和色素沉着。
淋巴结病症:约有30%~40%的患者伴发淋巴结病变。
肾脏病症:木村病患者中约12%~16%的病变累及肾脏,可表现为肾病综合征。肾脏病变可在皮下肿物出现后发生(较多见),也可同时发生。
其他症状:部分患者还伴有湿疹、哮喘、溃疡性结肠炎、血管炎、嗜酸性心肌炎、嗜酸性脂膜炎、分泌性中耳炎,同时可观察到有雷诺现象。
(三)诊断
根据临床表现及外周血嗜酸性粒细胞和IgE水平升高,亚裔患者应考虑木村病的可能。伴发肾脏疾病的患者中,可能有IgG4升高、血沉加快、白细胞增多、C反应蛋白升高等现象。
影像学检查可了解病变部位、血管情况、与周围组织关系。
①超声表现为软组织内边界不清楚的肿块,形态不规则,回声不均匀,可见条状高回声分布于低回声内,称为“木纹样”改变,部分与皮肤分界不清。
②CDFI:血流丰富,常伴有周围多发淋巴结肿大,肿大淋巴结主要表现为皮质增厚,淋巴门缩小或显示不清,内回声不均,可见多发微小的更低回声区域,血流既可以呈门型丰富血流,也可以紊乱。
③术前的CT和MRI有助于行病灶切除时的定位及明确肿物对周围软组织的累及范围。
病理学诊断
木村病需依靠活组织病理检查确诊(图3)。其特点如下:
①病变多呈灰黄或灰白色,病变无被膜,与周围组织无明显边界。
② 病变侵犯真皮层和肌肉;
③炎症细胞增生和浸润,病变组织可见广泛的淋巴滤泡样结构,大量的嗜酸性粒细胞、 淋巴细胞及肥大细胞充斥于滤泡间,多形成嗜酸性微脓肿(特征性改变);
④血管增生反应;
⑤不同程度的纤维化;
⑥免疫组化:淋巴滤泡以B细胞为主,而滤泡间以T细胞为主,生发中心内的嗜伊红色沉积物主要为IgE。

图3. 木村病的典型病理表现
对于多部位受累的木村病患者,存在活检病理部位的选择问题。头颈部作为常见受累部位,是活检首选部位,但却因为可能影响容貌,容易受到患者抵触。腹股沟淋巴结也是木村病的常见受累部位,且活检相对安全,但腹股沟淋巴结肿大特异性差,故在临床中常不被推荐。
2019年北京协和医院对46例患者的回顾性研究中,共17例因淋巴结活检确诊,其中7例(41.2%)通过腹股沟淋巴结活检确诊木村病,这一结果提示木村病患者中腹股沟淋巴结受累阳性率并不低,且因为其安全性可作为活检的首选。
(四)鉴别诊断
对于淋巴结肿大患者应注意区分病因,包括:感染、肿瘤、反应性增生、细胞代谢异常等。
有代表性的几种疾病如下:
血管淋巴样增生伴嗜酸性粒细胞增多症(ALHE):好发于头颈部,多表现为丘疹或红色结节,是一种良性血管增生性病变。ALHE与木村病非常相似,但ALHE病理以血管增生病变为主,增生的血管内皮细胞呈特征性的上皮样,而淋巴滤泡少见。
淋巴结结核:有淋巴结肿大、低热、盗汗等结核感染中毒症状,血沉增快,PPD试验强阳性,T-spot阳性,淋巴结病理可见干酪样坏死灶,抗酸染色阳性。
淋巴瘤:可表现为淋巴结肿大,伴有发热、乏力、体重明显下降,乳酸脱氢酶明显升高等,淋巴结病理可见淋巴结结构破坏,单克隆性B或T淋巴细胞增生,霍奇金淋巴瘤可见镜影细胞。
Castelman病:是一种淋巴增殖性疾病,表现为单发或全身多发的淋巴结肿大,其中颈部肿大淋巴结发生率较高,无嗜酸性粒细胞增多、IgE升高表现,淋巴结病理可见特征性“洋葱皮”样外观及“棒棒糖”结构。
血管免疫母细胞性淋巴结病:可表现为淋巴结肿大,但多为全身,且伴有发热、肝脾肿大、皮肤损害、高丙种球蛋白血症等表现。淋巴结病理可见淋巴结结构破坏,树枝状小血管增生伴内皮细胞增生肿胀。
(五)治疗
1.手术治疗
手术治疗是症状性患者的一线治疗,主要用于肿瘤减积或取材活检。由于其浸润性生长、界限不清,手术切除难以达到切缘阴性,导致手术切除术后复发率高,约为25%。
2.药物治疗
包括全身或局部的激素治疗、非甾体抗炎药、细胞毒性药物、环孢素、硫唑嘌呤、伊马替尼、免疫球蛋白等,疗效不一。
奥马珠单抗是一种抗IgE单克隆抗体,Nonaka等报告使用奥马珠单抗治疗3例手术治疗无法控制的KD患者获得成功,肿块体积缩小,外周血嗜酸性粒细胞和嗜碱性粒细胞计数减少。
3.生物制剂
Huang HY等在2022年首次报告一例伴有腹部和小腿慢性湿疹的36岁男性患者因左股部进行性增大的肿块接受手术切除,术后诊断为KD,患者接受了度普利尤单抗治疗8个月(初始600 mg,此后每2周300 mg),治疗4个月时皮损显著缩小,随访1年未复发。
Bellinato F等报告一例59岁塞内加尔男性KD患者病程长达20年,曾多次接受糖皮质激素、四环素类、吲哚美辛和氨苯砜治疗无效,实验室检查示外周血嗜酸性粒细胞百分数(15%)和血清IgE水平(800 UI/mL)升高。患者接受了度普利尤单抗300 mg皮下注射,每2周一次,治疗2个月后瘙痒完全缓解,皮下结节逐渐变平,遗留色素沉着,6个月随访未复发。
4.放射治疗
对于停用糖皮质激素后再次复发的病例,或肿物已对糖皮质激素产生耐药性的病例,可以考虑使用放射治疗。
对病变范围广、多发且边界不清的患者,首选放疗,而且对术后或放疗后复发的患者,再次放疗仍有效。
放射治疗的副作用较多,应尽量避免应用于年轻患者。
5.其他治疗
例如激光、冷冻试验性治疗。
(六)预后
该病属于良性病变,预后较好,但有较高复发率。
复发可能受多种因素的影响,如病程、病变大小、单发或多发、病变边界的清晰程度、外周血嗜酸性粒细胞及IgE水平。
有研究报道,病变范围>3.5 cm,外周血嗜酸性粒细胞百分比>50%,血IgE>10 000 IU/ml,Notch-1表达阳性或Ki-67增多的病人更容易复发,Notch-1和Ki-67可能是该病复发的预测指标。
二、木村病相关肾损害
木村病合并肾脏受累并不少见,12%~16%的患者有蛋白尿,其中59%~100%可表现为肾病综合征。肾损害常出现在木村病的肾外表现之后或同时发生。
目前所报道的木村病相关的肾损害病理类型多种多样,包括膜性肾病、微小病变性肾病、系膜增生性肾小球肾炎、局灶节段硬化性肾小球病、IgM或IgA肾病等,缺乏特异性。有个案报道肾活检可见部分伴有间质小管中单个核细胞和嗜酸性粒细胞浸润。
(一)木村病相关肾损害的病因及发病机制
有研究发现,伴有肾脏受累的木村病患者外周血CD4+和CD8+T细胞计数明显升高,提示辅助T细胞(Th细胞)参与疾病的发生发展过程。Th2分泌的白细胞介素4可诱导嗜酸性粒细胞聚集,并促进B细胞产生IgE。血嗜酸性粒细胞升高及高水平IgE引起的高敏状态可进一步干扰Th2细胞功能,并释放多种细胞因子,导致足细胞内相关信号通路活化,破坏足细胞骨架蛋白结构和细胞间连接蛋白,增加肾小球基底膜的通透性,引起蛋白尿。
(二)木村病相关肾损害的鉴别诊断
肾病综合征合并淋巴结肿大其他病因需鉴别如下:
1.淋巴增殖性疾病:包括淋巴瘤、Castleman病、POEMS综合征等。
淋巴瘤:常有发热、盗汗、体重减轻等表现,肝脾可肿大,组织病理可协助鉴别; Castleman病可有发热、乏力、红细胞沉降率增快等表现,常伴IL-6、VEGF水平升高,组织病理可协助鉴别;
POEMS综合征:该病诊断以多发神经病变、单克隆免疫球蛋白血症为必要条件,伴有皮肤及内分泌病变。
2.自身免疫疾病
自身免疫疾病可有乏力、口干、眼干、皮疹、关节疼痛等表现,且多表现为多系统受累,血中可检测到特异性自身免疫抗体。
3.实体肿瘤
实体肿瘤多见于老年人,可有体重减轻、贫血等消耗症状,可有肿瘤标记物的升高,影像学检查可发现实体肿瘤灶。
4.IgG4相关疾病
常表现为自身免疫性胰腺炎、硬化性胆管炎和/或唾液腺、泪腺肿大,伴血IgG4升高,组织病理学检查发现密集淋巴浆细胞浸润、席纹状纤维化和闭塞性静脉炎是主要诊断特征。
5.感染性疾病
常有发热及其他系统感染的表现,如咳嗽、咳痰、腹痛、腹泻、皮肤红肿等,常伴有炎症指标升高,病原学检查阳性。
(三)木村病相关肾损害的治疗
木村病合并肾病综合征患者首选全身应用激素治疗,对于复发或激素耐药患者需应用激素联合免疫抑制剂治疗。
为预防木村病复发或有肾脏等其他脏器受累,部分病例报道在糖皮质激素减量时,可加用免疫抑制剂,常用免疫抑制剂包括环磷酰胺、吗替麦考酚酯、环孢素、他克莫司等。
也有在个别肾脏受累患者中发现,即使联合糖皮质激素及免疫抑制剂仍可能无法有效控制病情,但当手术切除皮下受累肿块后,患者的膜性肾病也可很快得到缓解。
专家简介

周晓霜 教授
山西省人民医院肾内科
主任医师,博士研究生导师,省优专家
肾脏重症病区主任
山西省肾脏病大数据中心常务副主任
医学博士,美国贝勒医学院肾内科博士后
太原理工大学大数据学院博士后
主持国家自然科学基金3项,主持山西省优秀青年基金
获 “中共山西省委组织部山西省青年拔尖人才”、 “山西省人民政府嘉奖” 、“山西省学术技术带头人”“三晋英才拔尖骨干人才”、“山西省五四青年奖章”、“山西省青年岗位能手”等荣誉。
- 推荐文章
揭秘BAFF、APRIL在IgA肾病中的作用以及治疗研究进展
2a期IGNAZ研究最终结果:Felzartamab持续减少IgA肾病患者蛋白尿并减缓eGFR下降 | WCN 2025
患者小课堂|肾功能的好与坏,谁说了算?
远离腹膜透析的“隐形杀手”!肾病透析患者继发于牙龈感染后的反复发作性腹膜炎
常染色体显性多囊肾病中的肾切除术:ERA基因和肾脏工作组的共识声明
迄今为止最大横断面研究显示:适量至大量饮用啤酒以及适量饮用葡萄酒与肾结石患病率降低显著相关
WCN高影响力临床试验 | Ⅲ期REGENCY试验结果公布——奥妥珠单抗治疗活动性狼疮性肾炎显著有效且安全
多维度研究结合AI、多组学分析助力钙化防御研究获突破,中国两项成果亮相WCN 2025
WCN高影响力临床试验 | 探索CKD孕妇新疗法:甜菜根汁或成关键?
河南省人民医院肾内科团队2项成果亮相WCN 2025,泽贝妥单抗治疗特发性膜性肾病前景广阔
WCN高影响力临床试验 | FLOW试验中不同CKD严重程度下司美格鲁肽的临床与安全性结果公布
WCN中国之声 | 北大医院崔昭教授团队研究揭示抗nephrin抗体在中国成人MCD与原发性FSGS患者中的临床意义
WCN中国之声 | 北大研究团队发布中国2型糖尿病合并CKD患者10年用药“全景图”
WCN 2025 | 预测CKD进展的冰火两重天:TGF-β亚型遭否定,贝叶斯深度学习算法或成新宠
WCN2025 | 新型药物Sparsentan一线治疗IgA肾病取得关键进展,SPARTAN试验的中期成果发布
WCN中国之声 | 血管钙化与自噬基因揭示糖尿病肾病潜在致病机制
WCN2025 | 醛固酮合酶抑制剂联合SGLT2抑制剂协同增效,显著降低CKD患者尿蛋白
WCN中国之声 | 郑大一附院肾脏内科医学部研究团队开辟维持糖尿病患者钾稳态的新视角
WCN 2025本地组织工作组主席解读:印度首次举办WCN的里程碑意义与愿景
苏大附一院两项研究亮相WCN 2025,助力早期识别CKD和预测脓毒症相关AKI进展
WCN中国之声 | AI+视网膜血管几何参数——解放军总医院研究团队构建糖尿病肾病无创诊断及预后预测模型
ISN主席谈WCN 2025的作用——肾脏病学发展的关键引擎
WCN 2025 | 中国学者研究揭示肾结石与脂代谢紊乱的遗传关联
WCN中国之声 | 李贵森教授团队揭秘控制CKD血管钙化的新靶点和FSGS足细胞损伤新机制
WCN中国之声 | 培莫沙肽治疗NDD-CKD贫血不劣于阿法依泊汀,更优铁剂利用
WCN中国之声 | 整合前沿生物信息学技术确定AKI新治疗靶点——来自中国香港学者的三项研究
年度盘点 | 杨琼琼教授:肾性贫血治疗指南与研究进展
年度盘点丨以 “精准导航” 为翼,探秘脓毒症相关AKI诊断新境
WCN 2025 | 创新肾类器官模型,为肾毒性筛查提供新方法
APCN前主席:IgA肾病东西方临床特征差异与未来治疗展望
T2DM合并CKD的分层管理策略:英国ABCD-UKKA联合指南要点概述
从发病机制到诊疗指导:遗传学研究为ADPKD诊疗带来新视野
2025 KDIGO ADPKD临床实践指南重磅公布:妊娠和生殖、儿童相关话题及患者管理方法(完结)
2025 KDIGO ADPKD临床实践指南重磅公布:ADPKD的肾外表现评估与管理以及生活方式干预篇(未完待续)
2025 KDIGO ADPKD临床实践指南重磅公布:治疗药物及管理方法篇(未完待续)
利妥昔单抗治疗成人肾病综合征的研究进展
医路“肾”行,智“会”指南——2025年肾脏病领域学术会议全览
ICCN 2024速递:利用大数据指导急性肾损伤管理
CCSN 2024丨周晓霜教授:基于大数据的CKD全程管理与预测模型研究
CCSN 2024丨阳晓教授:腹膜透析治疗,发展与机会并存
CCSN 2024丨国际IgA肾病领军者专访:解读KDIGO指南更新,明晰IgA肾病管理新动向
CCSN 2024丨杨琼琼教授:从代谢视角探索心肾共治的新策略
“对因治疗”又添新证据——布地奈德肠溶胶囊靶向肠道、直击病因,抑制下游补体系统的激活,对全身免疫系统无影响丨ASN 2024
ASN 2024中国之声 | 南方医院秦献辉教授团队:高PURE评分与较低的CKD风险相关
ASN中国之声 | 肾病瘙痒领域再添新药,中国原研外周选择性κ阿片受体激动剂(HSK21542)Ⅲ期结果首次公布!
Kidney Week 2024 | 10月27日,今日聚焦:全体会议ASN中期职业生涯奖颁奖,激励英才展望未来
ASN 2024丨真实世界数据提示IgA肾病患者早诊、早治、早获益!
CCSN 2024丨罗朋立教授:腹透相关性感染性腹膜炎对心血管不良事件的影响及防治策略
CCSN 2024丨中外大咖齐聚中华肾年会,共同绘制IgA肾病治疗新蓝图
CCSN 2024丨徐钢教授:细胞外囊泡递药系统在肾脏病中的应用探索
CCSN 2024丨周晓玲教授:肿瘤免疫治疗相关肾损害的机制、流行病学及应对策略
CCSN 2024丨刘军教授:单克隆免疫球蛋白相关肾损害(MGRS)的诊断思路和方法
CCSN 2024丨涂晓文教授:脓毒症相关急性肾损伤CRRT启动时机的探讨
关节痛也会导致肾受伤吗?自身免疫性疾病之类风湿性关节炎与肾脏的“亲密”关系
李贵森教授:全面梳理IgAN的治疗进展
