- 首页 > 正文
年度盘点 | 杨琼琼教授:肾性贫血治疗指南与研究进展
肾医线 发表时间:2025-02-17 13:13:50
杨琼琼 韦肖娜
中山大学孙逸仙纪念医院
肾性贫血是指各种肾脏疾病导致红细胞生成素(EPO)绝对或相对生成不足,以及尿毒症毒素影响红细胞生成及其寿命而发生的贫血。慢性肾脏病(CKD)患者贫血患病率显著高于普通人群,并随着 CKD进展而增加,透析患者贫血患病率高达91.6%~98.2%。贫血影响肾脏疾病患者的生活质量,增加肾脏疾病进展、终末期肾脏病(ESRD)、心血管事件及死亡的风险。因此及时诊断肾性贫血与有效治疗对患者意义重大。
肾性贫血的诊断需要系统规范地检查和评估,才能进行正确诊断。《中国肾性贫血诊治临床实践指南》建议推荐,对CKD 3期以上患者应常规进行贫血筛查[1]。肾性贫血的诊断流程如图1所示。
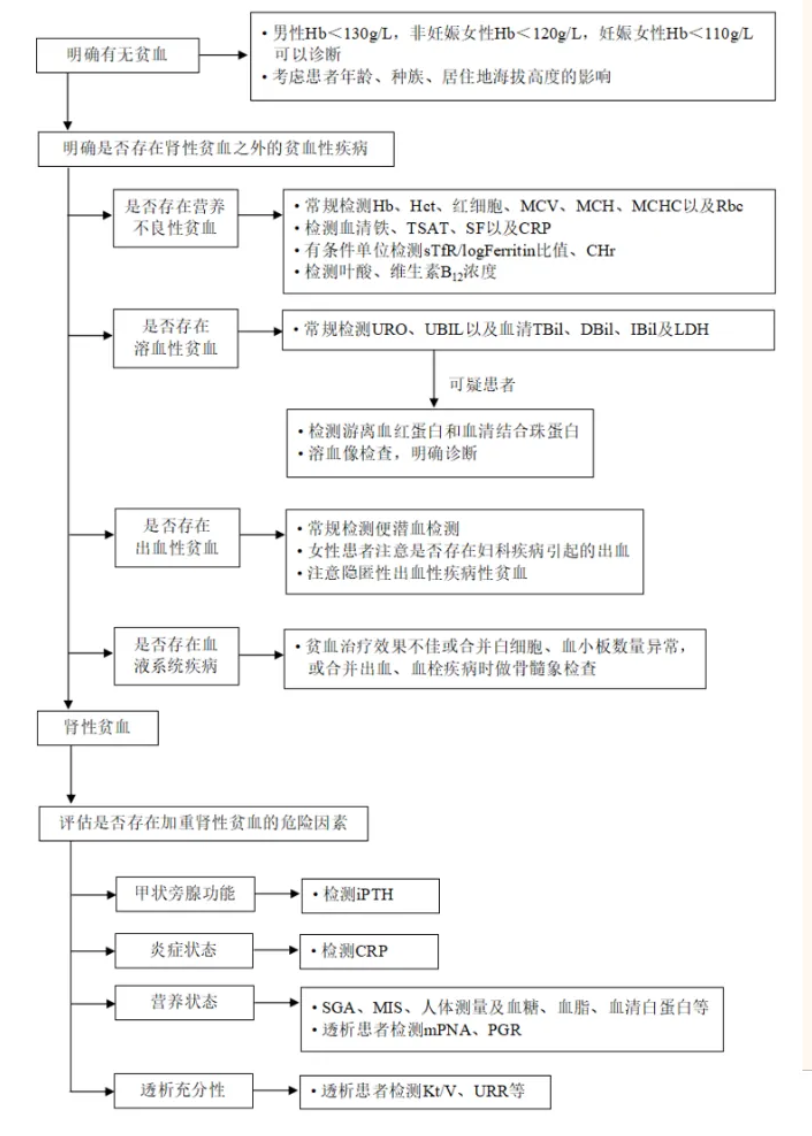
图1. 肾性贫血诊断流程与检测指标
目前临床上肾性贫血主要治疗药物包括3类:铁剂、红细胞生成刺激剂(ESAs)、低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI)。随着铁代谢在肾性贫血中的深入研究,发现铁调素-膜铁转运蛋白(FPN)轴是机体维持铁稳态的核心,任何影响铁调素-FPN轴的因素均会导致铁代谢相关疾病,包括肾性贫血的发生。因此,调节铁调素的多种药物将是未来肾性贫血治疗的新选择。《中国肾性贫血诊治临床实践指南》建议肾性贫血治疗的Hb靶目标为:Hb≥110 g/L,但不超过130 g/L;应根据患者的年龄、透析方式、生理需求及并发症情况,个体化调整Hb靶目标[1]。
1.铁剂
纠正铁缺乏是肾性贫血的关键治疗措施,将机体铁代谢维持在一个合理水平,以确保 ESAs 治疗反应性,降低CKD贫血导致的不良临床预后,改善患者生存率和生活质量。开始铁剂治疗前,首先评价Hb水平和铁代谢状态,寻找铁缺乏原因。存在绝对铁缺乏的 CKD 贫血患者,无论是否接受ESAs治疗,均应开始铁剂治疗,以满足红细胞生成的需求并防止铁缺乏加重。2025年KDIGO CKD贫血临床实践指南推荐草案指出,CKD血液透析(CKD G5HD)贫血患者,建议铁蛋白≤500 ng/ml(≤500 μg/L)和TSAT≤30%启动铁剂治疗。CKD未透析或腹膜透析(CKD G5PD)铁蛋白<100 ng/ml(<100 μg/L),TSAT<40%,或铁蛋白≥100 ng/ml(≥100 μg/L)和<300 ng/ml(<300 μg/L),TSAT <25%启动铁剂治疗。避免在活动性全身感染与持续菌血症患者中使用静脉铁剂[2]。
铁剂可分为口服铁剂和静脉铁剂两类。口服铁剂因方便性在国内被广泛使用,包括硫酸亚铁、蔗糖铁和柠檬酸铁铵等,但口服铁剂存在生物利用度低、胃肠道反应多和纠正贫血速度慢的问题。静脉铁剂能快速提升铁水平,在纠正贫血的效率上有显著优势,静脉铁剂不断发展与升级,最新的静脉铁剂可高剂量低频次使用。FERWON- NEPHRO研究比较单剂量异麦芽糖酐铁(1000 mg)与多次蔗糖铁静脉(200 mg/次,共2周,最多五次)改善CKD贫血的疗效,结果表明异麦芽糖酐治疗8周可有效纠正贫血,超敏反应发生率相对较低,复合心血管不良反应的发生率显著降低[3]。一项针对中国缺铁性贫血患者静脉注射羧基麦芽糖铁(最多两次,单剂量500或1000 mg)与蔗糖铁(200mg/次,最多11次)的随机、对照、开放标签非劣效性试验证实羧基麦芽糖铁治疗IDA的有效方法,能够更快地实现Hb反应和纠正铁缺乏,且输注次数少于蔗糖铁[4]。值得注意,《中国肾性贫血诊治临床实践指南》指出,在临床实践中应结合患者贫血和铁缺乏严重程度、治疗依从性以及静脉通路等因素,综合考量决定透析前CKD和腹膜透析患者铁剂治疗选择口服或静脉途径[1]。
2.ESAs
EPO不足为肾性贫血主要病因,补充EPO在CKD患者抗贫血治疗中具有非常重要的作用。ESA是EPO的类似物,目前ESA有短效ESA、长效ESA和持续性EPO受体激活剂(CERA)3种类型。ESAs可以有效纠正肾性贫血,但在使用前应尽可能地纠正铁缺乏或炎症状态等可能加重肾性贫血的危险因素。2025年 KDIGO CKD贫血临床实践指南推荐草案指出,CKD G5D血液透析(HD)或腹膜透析(PD)贫血患者,建议血红蛋白浓度 ≤90~100 g/L时启动ESA治疗。患者对ESAs的反应有较大个体化差异,ESA初始剂量应依据患者血红蛋白浓度、体重和临床情况决定,血红蛋白水平控制在115 g/L以下。应每2~4周监测一次Hb并相应调整剂量,避免血红蛋白快速上升>10 g/L[2]。
甲氧聚二醇重组人促红素注射液是首个持续性促红细胞生成素受体激动剂(continuous erythropoietin receptor activator,CERA)药物,每月使用1次,可大幅度提高患者的依从性,该药2007年被FDA批准,2024年在中国首次应用。新型长效EPO模拟肽——培莫沙肽是目前全球唯一的EPO模拟肽。一项培莫沙肽针对CKD透析贫血患者的随机对照、开放标签、非劣效性Ⅲ期临床试验结果表明,每月1次皮下注射培莫沙肽治疗中国透析患者的贫血疗效和安全性与常规每周1~3次α依泊汀相当[5]。培莫沙肽于2024年2月纳入《长效红细胞生成刺激剂治疗肾性贫血中国专家共识(2024年版)》。但需注意的是,ESAs的使用也增加了心血管不良事件发生包括心血管疾病基础上血压的升高及心脏病的加重,潜在促进肿瘤生长风险增加、血栓形成脑卒中的发生、感染风险上升、癫痫发作等[6]。
3.HIF-PHI
HIP-PHI药物是一类治疗肾性贫血的新型小分子口服药物,可促进生理范围内促红细胞生成素(EPO)生成,同时下调铁调素水平,增加机体对铁的吸收、转运和利用,减少铁剂用量。2025年 KDIGO CKD贫血临床实践指南推荐草案指出,ESA反应性低下患者,勿联合ESA和HIF-PHI。HIF-PHI治疗CKD贫血患者,不要超过最大推荐剂量,应以改善贫血症状和避免红细胞输注所需的最低剂量给予HIF-PHIs。应在启动HIF-PHI治疗或剂量改变后2~4周监测血红蛋白水平,随后治疗期间每4周监测一次。若未达到红细胞生成预期反应,则于3~4个月后停止HIF-PHI。在HIF-PHI治疗期间应全程监测铁代谢状态,必要时联合铁剂治疗[2]。2024年《HIF-PHI用于慢性肾脏病相关贫血:ERA欧洲肾脏最佳实践委员会文件》指出:(1)HIF-PHI谨慎应用包括血栓性并发症风险高的血管通路、视网膜疾病、自身免疫性疾病、有恶性肿瘤治愈史或至少5年未复发的患者,以及肾移植受者;(2)HIF-PHI避免使用或极其谨慎使用包括在过去3个月内经历过心血管事件或血栓性事件的患者、在过去5年内有恶性肿瘤史、囊性肾病、未经治疗的增殖性糖尿病视网膜病变、黄斑变性、视网膜静脉阻塞,以及特发性肺动脉高压的患者[7]。
罗沙司他2018年12月在我国被批准用于治疗CKD肾性贫血,2021年被我国肾性贫血诊治临床实践指南推荐为一线治疗用药。恩那度司他是第二个进入中国的HIF-PHI类药物,中国Ⅲ期临床数据表明恩那度司他在疗效、安全性、依从性上均有良好表现,有效实现Hb高达标率,Hb升速稳定,调药次数较少,服药安全便捷等临床需求,或可成为肾性贫血治疗优选[8]。目前达普度司他、莫利度司他、德度司他、伐达度司他等多种新型HIF-PHI药物的临床试验正在进行,为CKD患者贫血治疗提供了新见解。
4.铁调素
铁调素是一种由肝脏产生的多肽类激素,主要通过抑制细胞内铁的转运来维持机体的铁稳态。铁调素水平的表达通过多种信号通路调节,目前,直接铁调素抑制剂、BMP/Amad 通路靶向治疗、JAK/STAT3通路靶向治疗、HIF-脯氨酰羟化酶抑制,可以抑制铁调素水平,调控铁稳态[9-11]。针对这些信号通路,铁调素的多种拮抗剂相继被研发,其拮抗机制主要包括:通过抑制铁调素的正调节或增强负调节来抑制铁调素的产生,以及通过直接抑制铁调素或调控铁调素-FPN轴来影响铁调素的功能。
IL-6通路主要是通过抑制铁调素的正调节,促进胃肠道铁吸收和储存铁的动员、利用。Ziltivekimab是一种全人源单克隆IL-6抗体。RESCUE研究数据结果发现,Ziltivekimab的抗炎治疗改善了3~5期CKD和系统性炎症患者的贫血标志物和铁稳态,表明其在贫血管理中可能具有一定的作用。这可能与其减少炎症对铁代谢和红细胞生成的干扰有关,从而提高Hb水平和铁利用效率[12]。Clazakizumab是一种高亲和力人源化单克隆抗体,可以靶向IL-6 配体并抑制下游信号通路。2024年ASN肾脏周会议上发布了POSIBIL6ESKD Ⅱb/Ⅲ期研究中的Ⅱb期结果,该研究旨在评估Clazakizumab对肾衰竭患者贫血和铁参数的影响。研究结果显示,与安慰剂相比,Clazakizumab治疗显著降低了铁调素水平,未来需要在Ⅲ期研究中进一步证实[13]。
5.小结
肾性贫血的发生机制复杂,涉及多种因素共同参与,是全球公共卫生的重要难题之一,其治疗措施不应仅仅局限于或依赖于ESA、HIF-PHI和铁剂的使用,应该进行个体化、多管齐下的管理,除了促进造血本身,还要纠正所有可逆贫血原因,从而使肾性贫血患者得到全面的诊治。肾性贫血治疗任重道远,治疗理念不断进步,期待新药能够为患者带来更多临床获益。

杨琼琼
中山大学孙逸仙纪念医院
- 主任医师、博士生导师、博士后合作导师
中山大学孙逸仙纪念医院肾内科主任
中华医学会肾脏病学分会委员
中国医师协会肾脏内科医师分会常务委员
中国老年保健医学研究会老年肾病防治分会副主任委员
IIgANN-China学术委员会委员
广东省医学会肾脏病学分会副主任委员
广东省医疗行业协会肾内科管理分会主任委员
《中华肾脏病杂志》编辑委员会委员
《国际泌尿系统杂志》编辑委员会委员
参考文献
1.中国医师协会肾脏内科医师分会肾性贫血指南工作组. 中国肾性贫血诊治临床实践指南 [J] . 中华医学杂志, 2021, 101(20) : 1463-1502.2.KDIGO 2025 CLINICAL PRACTICE GUIDELINE FOR ANEMIA INCHRONIC KIDNEYDISEASE(CKD) PUBLIC REVIEWDRAFTNOVEMBER 2024.3.Sunil Bhandari, Philip A Kalra, Mario Berkowitz, et al. Safety and efficacy of iron isomaltoside 1000/ferric derisomaltose versus iron sucrose in patients with chronic kidney disease: the FERWON-NEPHRO randomized, open-label, comparative trial. Nephrol Dial Transplant. 2021;36(1):111-120.4.Jie Jin, Zhihua Ran, Emanuele Noseda, et al. A randomized, controlled, open label non-inferiority trial of intravenous ferric carboxymaltose versus iron sucrose in patients with iron deficiency anemia in China. Front Med. 2024;18(1):98-108.5.Ping Zhang, Yan Jiang, Chunping Xu, et al. Pegmolesatide for the treatment of anemia in patients undergoing dialysis:a randomized clinical trial. EClinicalMedicine. 2023; 65 102273.6.Chung EY, Palmer SC, Saglimbene VM, et al. Erythropoiesis-stimulating agents for anaemia in adults with chronic kidney disease: a network meta-analysis. Cochrane Database Syst Rev. 2023;2(2):CD010590. Published 2023 Feb 13.7.Stoumpos S, Crowe K, Sarafidis P, et al. Hypoxia-inducible factor prolyl hydroxylase inhibitors for anaemia in chronic kidney disease: a document by the European Renal Best Practice board of the European Renal Association. Nephrol Dial Transplant. 2024 Apr 4:gfae075.8.Liang X-L, Huang R-W, Xie J-T, et al. Enarodustat for the Treatment of Anemia in Chinese Patients with Non-Dialysis Chronic Kidney Disease: A Phase 3 Trial. Kidney Dis, DOI: 10.1159/000543193 (Published online).9.Ganz T, Nemeth E. Iron Balance and the Role of Hepcidin in Chronic Kidney Disease. Semin Nephrol. 2016,36(2):87-93.10.Pagani A, Nai A, Silvestri L, et al. Hepcidin and Anemia: A Tight Relationship. Front Physiol. 2019,9(10):1294.11.Bazeley JW, Wish JB. Recent and Emerging Therapies for Iron Deficiency in Anemia of CKD: A Review. Am J Kidney Dis. 2022;79(6):868-876.12.Pablo E Pergola, Michael Davidson, Camilla Jensen, et al. Effect of Ziltivekimab on Determinants of Hemoglobin in Patients with CKD Stage 3-5: An Analysis of a Randomized Trial (RESCUE). J Am Soc Nephrol. 2024 Jan 1;35(1):74-84.13.Neuen Brendon Lange, Wolf Myles, Catanese Benjamin Peter, et al. Effects of Interleukin-6 Inhibition with Clazakizumab on Anemia and Iron Parameters in Patients with Kidney Failure. ASN 2024. TH-PO875.
- 推荐文章
揭秘BAFF、APRIL在IgA肾病中的作用以及治疗研究进展
2a期IGNAZ研究最终结果:Felzartamab持续减少IgA肾病患者蛋白尿并减缓eGFR下降 | WCN 2025
患者小课堂|肾功能的好与坏,谁说了算?
远离腹膜透析的“隐形杀手”!肾病透析患者继发于牙龈感染后的反复发作性腹膜炎
常染色体显性多囊肾病中的肾切除术:ERA基因和肾脏工作组的共识声明
迄今为止最大横断面研究显示:适量至大量饮用啤酒以及适量饮用葡萄酒与肾结石患病率降低显著相关
WCN高影响力临床试验 | Ⅲ期REGENCY试验结果公布——奥妥珠单抗治疗活动性狼疮性肾炎显著有效且安全
多维度研究结合AI、多组学分析助力钙化防御研究获突破,中国两项成果亮相WCN 2025
WCN高影响力临床试验 | 探索CKD孕妇新疗法:甜菜根汁或成关键?
河南省人民医院肾内科团队2项成果亮相WCN 2025,泽贝妥单抗治疗特发性膜性肾病前景广阔
WCN高影响力临床试验 | FLOW试验中不同CKD严重程度下司美格鲁肽的临床与安全性结果公布
WCN中国之声 | 北大医院崔昭教授团队研究揭示抗nephrin抗体在中国成人MCD与原发性FSGS患者中的临床意义
WCN中国之声 | 北大研究团队发布中国2型糖尿病合并CKD患者10年用药“全景图”
WCN 2025 | 预测CKD进展的冰火两重天:TGF-β亚型遭否定,贝叶斯深度学习算法或成新宠
WCN2025 | 新型药物Sparsentan一线治疗IgA肾病取得关键进展,SPARTAN试验的中期成果发布
WCN中国之声 | 血管钙化与自噬基因揭示糖尿病肾病潜在致病机制
WCN2025 | 醛固酮合酶抑制剂联合SGLT2抑制剂协同增效,显著降低CKD患者尿蛋白
WCN中国之声 | 郑大一附院肾脏内科医学部研究团队开辟维持糖尿病患者钾稳态的新视角
WCN 2025本地组织工作组主席解读:印度首次举办WCN的里程碑意义与愿景
苏大附一院两项研究亮相WCN 2025,助力早期识别CKD和预测脓毒症相关AKI进展
WCN中国之声 | AI+视网膜血管几何参数——解放军总医院研究团队构建糖尿病肾病无创诊断及预后预测模型
ISN主席谈WCN 2025的作用——肾脏病学发展的关键引擎
WCN 2025 | 中国学者研究揭示肾结石与脂代谢紊乱的遗传关联
WCN中国之声 | 李贵森教授团队揭秘控制CKD血管钙化的新靶点和FSGS足细胞损伤新机制
WCN中国之声 | 培莫沙肽治疗NDD-CKD贫血不劣于阿法依泊汀,更优铁剂利用
WCN中国之声 | 整合前沿生物信息学技术确定AKI新治疗靶点——来自中国香港学者的三项研究
年度盘点 | 杨琼琼教授:肾性贫血治疗指南与研究进展
年度盘点丨以 “精准导航” 为翼,探秘脓毒症相关AKI诊断新境
WCN 2025 | 创新肾类器官模型,为肾毒性筛查提供新方法
APCN前主席:IgA肾病东西方临床特征差异与未来治疗展望
T2DM合并CKD的分层管理策略:英国ABCD-UKKA联合指南要点概述
从发病机制到诊疗指导:遗传学研究为ADPKD诊疗带来新视野
2025 KDIGO ADPKD临床实践指南重磅公布:妊娠和生殖、儿童相关话题及患者管理方法(完结)
2025 KDIGO ADPKD临床实践指南重磅公布:ADPKD的肾外表现评估与管理以及生活方式干预篇(未完待续)
2025 KDIGO ADPKD临床实践指南重磅公布:治疗药物及管理方法篇(未完待续)
利妥昔单抗治疗成人肾病综合征的研究进展
医路“肾”行,智“会”指南——2025年肾脏病领域学术会议全览
ICCN 2024速递:利用大数据指导急性肾损伤管理
CCSN 2024丨周晓霜教授:基于大数据的CKD全程管理与预测模型研究
CCSN 2024丨阳晓教授:腹膜透析治疗,发展与机会并存
CCSN 2024丨国际IgA肾病领军者专访:解读KDIGO指南更新,明晰IgA肾病管理新动向
CCSN 2024丨杨琼琼教授:从代谢视角探索心肾共治的新策略
“对因治疗”又添新证据——布地奈德肠溶胶囊靶向肠道、直击病因,抑制下游补体系统的激活,对全身免疫系统无影响丨ASN 2024
ASN 2024中国之声 | 南方医院秦献辉教授团队:高PURE评分与较低的CKD风险相关
ASN中国之声 | 肾病瘙痒领域再添新药,中国原研外周选择性κ阿片受体激动剂(HSK21542)Ⅲ期结果首次公布!
Kidney Week 2024 | 10月27日,今日聚焦:全体会议ASN中期职业生涯奖颁奖,激励英才展望未来
ASN 2024丨真实世界数据提示IgA肾病患者早诊、早治、早获益!
CCSN 2024丨罗朋立教授:腹透相关性感染性腹膜炎对心血管不良事件的影响及防治策略
CCSN 2024丨中外大咖齐聚中华肾年会,共同绘制IgA肾病治疗新蓝图
CCSN 2024丨徐钢教授:细胞外囊泡递药系统在肾脏病中的应用探索
CCSN 2024丨周晓玲教授:肿瘤免疫治疗相关肾损害的机制、流行病学及应对策略
CCSN 2024丨刘军教授:单克隆免疫球蛋白相关肾损害(MGRS)的诊断思路和方法
CCSN 2024丨涂晓文教授:脓毒症相关急性肾损伤CRRT启动时机的探讨
关节痛也会导致肾受伤吗?自身免疫性疾病之类风湿性关节炎与肾脏的“亲密”关系
李贵森教授:全面梳理IgAN的治疗进展
